营养性肥胖大鼠血浆胰岛素水平变化
作者;李襄,张咏梅,李倩,桂明红,汪振兴,余上斌,冯秀玲,熊宗斌
【摘要】 目的 观测营养性肥胖大鼠血浆胰岛素水平变化。方法 实验分为普通饲料喂养大鼠组(A组),高能饲料喂养大鼠组(B组),大鼠肥胖抵抗组(C组);采用放射免疫法检测血浆中胰岛素浓度;并称量各组大鼠不同时段体重。结果 B组动物血浆胰岛素水平(51.82±13.52)mU/L高于A组(29.37±12.88)mU/L (P<0.01),而与C组(49.88±18.71)mU/L差异无显著性(P>0.05); C组(49.88±18.71)mU/L高于A组(29.37±12.88)mU/L(P<0.01)。结论 营养性肥胖大鼠血浆胰岛素水平明显升高,表明肥胖症大鼠存在胰岛素抵抗;并提示高脂饮食对胰岛素抵抗的诱导作用可能与体重增长不相关联。
【关键词】 肥胖症;胰岛素;体重
Changes of insulin level in nutrient obesity rats
【Abstract】 Objective To observe the changes of plasma insulin level in nutrient obesity rats.Methods Experiment group: normal food fed Group A,high fat diet Group B,obesity resistant Group C.The concentration of insulin was detected by radioimmunoassy.The body weight of rats were measured and calculated respectively.Results The plasma insulin level in obesity rats Group B (51.82±13.52)mU/L was higher than that in normally-fed rats Group A (29.3712.88)mU/L(P<0.01),but no obvious difference with that of the obesity resistant Group C ( 49.88±18.71) (P>0.05).Plasma insulin level in Group C (49.88±18.71)mU/L was higher than Group A(29.37 ±12.88)mU/L(P<0.01).Conclusion The plasma insulin level increased obviously in the nutrient obesity rats,compared to the normal control group,indicates the high fat diet induce the insulin resistant effect.For the obesity resistant group,indicating the insulin resistant effect induced by high fat diet may not concerned with the growth of body weight.
【Key words】 obesity; insulin; weight
胰岛素(insulin)是由胰岛β细胞所分泌的一种相对分子质量为56000的酸性蛋白质,由含21个氨基酸的A1链和含30个氨基酸的B链通过二硫键相连。其生理作用:(1)糖代谢方面:可以增加葡萄糖的转运,加速葡萄糖的酵解和氧化,促进糖原的合成和储存,同时又抑制糖原的分解和异生,使血糖的利用增加而来源减少,从而降低血糖。(2)脂肪代谢:能增加脂肪酸的转运,促进脂肪的合成并抑制其分解,从而减少非酯化脂肪酸和酮体的生成。(3)蛋白质代谢:可增加氨基酸的转运,促进蛋白质的合成,同时又抑制蛋白质的分解。(4)钾离子转运:促进钾离子的内流,增高细胞内钾离子浓度。(5)促进生长作用:胰岛素的结构和胰岛素样生长因子(IGF)相似,已从人血中分离出IGF-1和IGF-2。各组织中均有IGF-1受体,胰岛素可与IGF-1受体结合,发挥促生长作用。胰岛素的促生长作用与促进蛋白质、脂肪和核酸的合成有关。
作为人体内降血糖的激素胰岛素的分泌受血糖的控制,血糖升高就会引起胰岛素分泌增多,血糖降低,分泌则减少。但是随着人们对肥胖研究的深入,发现胰岛素抵抗(IR)作用,是糖尿病、高血压及脂代谢紊乱发生的基础[1]。这种胰岛素抵抗作用还可以通过一定的方式来改善,有研究证实通过补充机体的铬离子可有效降低糖尿病病人体内胰岛素水平,提高胰岛素敏感性,改善胰岛素抵抗作用,从而明显降低IR相关疾病的危险性[2,3]。本实验旨在探讨营养性肥胖大鼠胰岛素水平变化。
1 材料与方法
1.1 实验动物 实验用初生1月龄健康雄性SD大鼠(由同济医学院实验动物中心提供),体重120~140g。室温(25±2)℃,维持12h/24h昼夜,饲料,自来水随意饮用,适应环境1周后,随机分为两组:普通饲料喂养组(A组,n=10只),高能饲料喂养组(B组,n=30只);喂养10周后,高能饲料喂养组动物体重超过对照组平均体重加三个标准差者[4],设为DIO组;体重未超过对照组平均体重的大鼠,设为肥胖抵抗组(diet resistant,DR),得肥胖抵抗组(C组,n=10只)。各组动物分笼喂养,3天记录1次体重。
1.2 动物饲料 标准动物饲料成分:5%脂肪,55%碳水化合物,22%蛋白质,7%灰分,5%纤维素,饲料热量为3.80kcal/g。由本校实验动物中心加工而成。高能饲料配方:50%标准动物饲料,15%猪油,10%白糖,5%奶粉,10%鸡蛋,5%芝麻油,5%花生仁,能量成分为:30%脂肪,40%碳水化合物,15.5%蛋白质,4%灰分,3%纤维素,饲料热量为4.76kcal/g[5]。
1.3 实验仪器 高速离心机(德国Sigma公司):SN-695B型智能放射免疫γ测量仪(上海原子核研究所日环仪器一厂);秤ES-C200A(湘仪天平仪器厂)。
1.4 血液检测 实验结束,去下腔静脉血,分别装入10ml塑料管,室温,3000rpm离心20min,取上清。送协和放射科放射免疫实验室测各样本血清内胰岛素浓度。
1.5 统计学方法 实验数据以x±s表示,实验结果t检验。
2 结果
2.1 各组大鼠体重变化 高能饲料喂养肥胖动物体重增长明显高于普通饲料喂养组、肥胖抵抗组;肥胖抵抗组动物体重高于普通饲料喂养组;肥胖抵抗组动物体重与高能饲料喂养肥胖组比较差异无显著性。结果见表1。
表1 各组大鼠体重比较 (x±s,n=10)
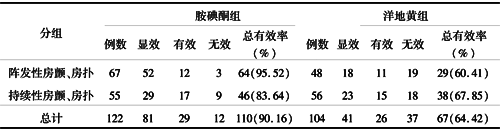
注:△P<0.05,*P<0.01 B vs A, #P<0.01 C vs A
2.2 各组大鼠血清胰岛素水平变化 高能饲料喂养组动物血浆胰岛素水平明显高于普通饲料喂养组;肥胖抵抗组大鼠血浆胰岛素水平明显高于普通饲料喂养组;肥胖抵抗组动物血浆胰岛素水平与肥胖组比较差异无显著性。结果见表2。
表2 各组大鼠血浆胰岛素水平比较 (x±s,n=10)
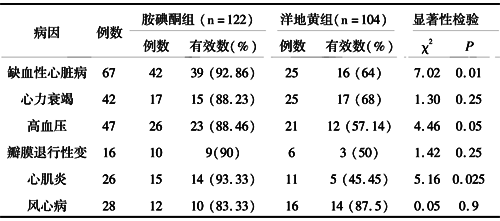
注:*P<0.01 B vs A, #P<0.01 C vs A
3 讨论
本实验结果显示,高能饲料喂养大鼠肥胖组(C组)在第4、8、12、16周时平均体重增长高于普通饲料喂养组(A组)(P<0.01);肥胖抵抗组(B组)仅在14周时平均体重增长高于普通饲料喂养组:表明高能饲料喂养大鼠发生了肥胖症。
高能饲料喂养组中肥胖组和肥胖抵抗组大鼠血浆胰岛素水平均明显高于普通饲料喂养组(P<0.01),验证肥胖大鼠体内胰岛素抵抗现象。
虽然肥胖引起IR的机制仍然是个尚未明确的课题。但随着对IR认识的深入,肥胖与IR之间的关系愈加备受关注。对于胰岛素抵抗机制的研究显示,胰岛素的生物效应分为两大类:它在胞浆内主要通过激活或抑制已存在的蛋白质(受体、酶、转录因子、信号蛋白等)起快速作用;而在核内,它通过调控基因转录及相应蛋白质的表达起缓慢作用。胰岛素受体具有内在的酪氨酸蛋白激酶活性,通过使其自身及胰岛素受体底物-1(IRS-1)磷酸化而介导细胞对胰岛素的反应,磷酸化了的IRS-1相当于第二信使,它与富含SH2的蛋白质磷脂酰肌醇-3(PI-3K)结合,使之激活,促进葡萄糖转运体-4(GLUT-4)的合成及由细胞内池迁移至细胞膜,启动细胞对葡萄糖的摄取。肥胖由于脂肪细胞大及数量增多,导致其分泌的激素的表达增强或减弱,从不同层次影响胰岛素的效应,从而导致IR。研究发现,脂肪细胞分泌的FFA[6],瘦素[7~9],肿瘤坏死因子 α(TNF-α ),抵抗素(resistin),脂联素(adiponectin)等与IR关系密切。而过氧化物酶体增殖体激活物受体γ (PPAR-γ )亦是肥胖导致IR的重要机制之一[1]。
亦有研究证明,肥胖大鼠外周血中同时存在胰岛素抵抗和高胰高血糖素现象,说明在肥胖大鼠中,外周IR的病理状态下胰高血糖素的分泌及合成功能亢进,胰岛素通过邻分泌作用抑制α细胞胰高血糖素分泌的负反馈机制,而这种负反馈机制是通过α细胞膜上的胰岛素受体的信号转导实现的。通过在胰岛细胞表面灌注可发现,肥胖大鼠基础胰岛素分泌高于正常,高浓度葡萄糖可刺激对照组胰岛β细胞胰岛素的Ⅰ相分泌,而在肥胖组这种Ⅰ相分泌刺激作用显著减弱。β细胞胰岛素信号转导对胰岛素的分泌和合成具有正反馈调节作用,选择性β细胞IRc基因敲除鼠也表现为胰岛素Ⅰ相分泌障碍,提示β细胞胰岛素信号转导障碍可能是胰岛素Ⅰ相分泌障碍的重要原因之一。高血糖可抑制对照组大鼠胰岛胰高血糖素的分泌,却不能抑制肥胖鼠胰高血糖素分泌。对于高脂饮食诱导的肥胖大鼠胰岛的胰岛素信号转导系统研究发现,胰岛存在IRc、IRS-1 和IRS-2的表达。外周存在IR的肥胖组,胰岛IRc表达明显降低,且同时伴有IRS-2表达的显著降低,表明胰岛的IR发生在受体和受体后水平,即由于其IRc和受体后转导的障碍所致,且IRc和IRS-2的表达降低遍及胰岛中心及岛幔(mantle)细胞,强烈提示β和α细胞胰岛素受体信号转导系统受损有关,亦即α和β细胞IR。这些研究结果都是“胰岛自身IR假说”的有力支持[10]。
【】
1 杨凌辉,邹大进.肥胖致胰岛素抵抗的机制.中华内分泌代谢杂志,2002,18(3):244-246.
2 李建飞,李志红,李玉林.微量元素铬与糖尿病.微量元素与健康研究,2002,19(3):73-74.
3 卫子然,游超,余上斌,等.铬对膳食诱导的肥胖大鼠血清中瘦素的影响,2001,35(4):237-239.
4 田德潤,李晓东,石玉顺,等.肥胖大鼠血浆摄食相关肽和血脂水平变化.天津医科大学学报,2004,3:10.
5 余上斌,刘声远.营养性肥胖大鼠肠系膜微循环变化。微循环,2005,9(1):41-42.
6 Bonden G.Role of fatty acids in the pathogenesis of insulin resistance and NIDDM.Diabetes,1997,46:3-10.
7 郑宪玲,张洪峰.瘦素与胰岛素抵抗.国外医学·内分泌分册,2001,21(5):256-257.
8 Widjaja A,Stratton IM,Horn R,et al.U KPDS 20: plasma leptin,obesity and plasma insulin in type 2 diabetic subjects.J Biol Chem,1998,273:18365-18373.
9 Walder K,Filipps A,Clark S,et al.Leptin inhibits insulin binding in isolated rat adipocytes.Endocrinol,1997,155:R5-R7.
10 邬云红,李秀钧,李宏亮.高脂饮食肥胖大鼠胰岛细胞胰岛素抵抗机理的探讨.中华医学杂志,2005,27:1607-1610.











