冷冻免疫生物治疗恶性黑色素瘤的临床研究
作者:王富水,黄宏春,王秀敏,张素芳,崔东海
【摘要】 目的 探讨恶性黑色素瘤患者应用冷冻免疫生物的临床意义。方法 对86例恶性黑色素瘤患者分别采用冷冻免疫生物治疗、常规手术切除或放疗加化疗,观察各组治疗前后免疫功能变化、T淋巴细胞亚群改变,并评价5年生存期。结果 治疗后冷冻免疫治疗组中位生存时间(MST,2年8个月)较标准治疗对照组(MST,1年8个月)明显升高(P均<0.05)。治疗后冷冻免疫治疗组CD4、CD4/CD8较治疗前及标准治疗对照组明显升高(P均<0.05)。而治疗后标准治疗对照组较治疗前血CD3、CD4水平、CD4/CD8比值显著下降(P均<0.05)。结论 冷冻免疫生物疗法可提高患者免疫功能,明显延长患者生存时间。
【关键词】 黑色素瘤;冷冻;生物疗法;瘤苗
恶性黑色素瘤(malignant melenoma,MM)发病率占人体恶性肿瘤的1%~2%,恶性程度较高,即使是Ⅰ期病变,也有11%的患者术后出现局部复发或远处转移[1]。对有复发或转移者应用含氮烯咪胺(DTIC)、顺铂(DDP)、卡莫司汀(BCNU)和三苯氧胺的联合化疗方案,虽有一定疗效,但对远期生存影响不大。近年来我们对恶性黑色素瘤患者应用冷冻免疫生物治疗,疗效较好,现报告如下。
1 资料与方法
1.1 一般资料 86例恶性黑色素瘤患者均为2000年4月~2002年4月我院与安阳市肿瘤收治的恶性黑色素瘤患者,男60例,女26例。年龄19~78岁,中位年龄45岁。肿瘤部位以头面部和四肢最多见(71.9%),躯干、消化道和生殖系统分别占11.0%、8.1%、6.5%。临床分期:Ⅰ期28例(32.6%);Ⅱ期37例(43.0%);Ⅲ期21例(24.4%)。
1.2 研究方法 随机选35例分入冷冻免疫生物治疗组。方法:(1)冷冻破坏术,采用液氮冷冻破坏术,一般采用接触法、喷射法和倾注浸泡法3种。1次冷冻包括3个快冻慢融周期,冷冻范围超过病灶1~1.5cm。(2)冷冻瘤苗埋藏术[2],冷冻破坏癌瘤后或切除癌瘤后冷冻灭活制成瘤苗,置无菌液氮罐中冷冻保存,定期进行冷冻瘤苗回植皮下埋藏术。短小棒状杆菌菌苗、卡介苗为佐剂。(3)生物治疗,INFα 300万u,sc,每周一、三、五用药;IL-2 200~400万u,im,每周二、四、六用药,共用药6~8周[3]。51例患者用常规手术切除或放疗加化疗等治疗方法为对照组,化学治疗药物以PDD、CBP和DTIC为主(PDD 100mg/m2,第1天;或CBP 350mg/m2,第1天;或DTIC 125mg/m2,第1~5天)。21~28天为1个周期,2~3周期为1个疗程。
1.3 观察指标 治疗前两组均进行免疫功能检查、T淋巴细胞亚群检测(CD43、CD4、CD48)。2个月后两组同时复查上述指标,并评价5年生存率。
1.4 统计学方法 采用社会统计分析软件包(SPSS 10.0)进行数据管理及统计分析。数值变量资料用均数±标准差(2 结果
2.1 冷冻免疫治疗恶性黑色素瘤对生存率的影响 见表1。冷冻免疫治疗组较标准治疗对照组中位存活时间显著延长(P均<0.05)。
表1 冷冻免疫治疗恶性黑色素瘤对生存率的影响
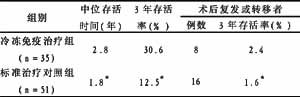
注:冷冻免疫治疗组υs标准治疗对照组,*P<0.001
2.2 冷冻免疫治疗恶性黑色素瘤对机体免疫功能的影响 见表2。应用冷冻免疫治疗后恶性黑色素瘤患者血CD3、CD4水平、CD4/CD8水平较治疗前显著升高(P均<0.001)。治疗后冷冻免疫治疗组较标准治疗对照组血CD3、CD4水平、CD4/CD8比值显著升高(P均<0.001)。治疗后标准治疗对照组较治疗前血CD3、CD4水平、CD4/CD8比值显著下降(P均<0.05)。
3 讨论
恶性黑色素瘤是一种少见的高度恶性肿瘤,可发生于身体任何部位,容易发生血行和(或)淋巴结转移,预后较差。恶性黑色素瘤发生与机体免疫功能状态有关。Mark[4]发现恶性黑色素瘤患者血清中存在能与自体或异体瘤组织特异性结合的自身抗体,少数患者的肿瘤有自发消退的现象,印证了恶性黑色素瘤与免疫过程的密切关系。因此提高机体的免疫应激能力,尤其是提高细胞免疫系统的功能是恶性黑色素瘤患者的重要环节[2,5]。
表2 冷冻免疫治疗恶性黑色素瘤对机体免疫功能的影响 (x±s)
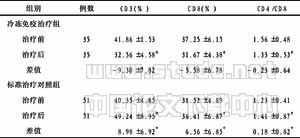
注:冷冻免疫治疗组υs标准治疗对照组治疗前后差值,*P<0.001(采用配对样本t检验);治疗后υs治疗前,#P<0.05(采用独立样本t检验)
我们采用冷冻免疫生物治疗恶性黑色素瘤治疗效果明显,结果显示此疗法可以提高患者中位生存率、3年生存率,明显优于标准治疗对照组(P<0.05)。我们的研究还提示冷冻免疫生物治疗恶性黑色素瘤能激发机体产生细胞免疫效应。近期研究发现恶性黑色素瘤患者具有能与其自身肿瘤抗原发生反应的致敏淋巴细胞;特异性主动免疫治疗能增强这种反应性,而不是重新诱导反应。肿瘤疫苗能诱导免疫记忆应答,从而加强对肿瘤细胞的免疫监视,减少显微转移灶形成[5]。汤钊猷[6]研究提示冷冻破坏癌细胞所引起的抗原的释放,比放射线、激光照射损害肿瘤细胞所引起的抗原释放都高,且这种免疫效应具有种属、器官、组织特异性。
本研究表明冷冻免疫生物疗法可提高患者生存率,为治疗恶性黑色素瘤探索出一条新的有效途径。但作为一种主动特异性的治疗手段,仍需进一步探寻免疫原性的特异性更高的疫苗制剂及研究免疫疫苗对恶性黑色素瘤主动特异免疫治疗的机制。
【】
1 李顺凡(译).人体恶性黑色素瘤.国外医学·皮肤病学分册,1998,2(12):93-94.
2 Hausen,Gruis NA,Weaver-Feldhaus J,et al.A cell cycleregulator potentially involveding enesisofmany tuner types.Science,1997,88:110.
3 Legha SS,Ring S,Eton O,et al.Development of a biochemotherapy regimen with concurrent administration of cisplatin,vinblasbine,dacarbazine,interferon alfa,and interleukin-2 for patients with metastatic melanoma.J Clin Oncol,1998,16(5):1752-1759.
4 Mark J.Howcell scycletowardcancer.Science,1994,263:319.
5 蒙志斌.冷冻免疫治疗恶性黑色素瘤新进展.医学文选,2001,20(5):705-706.
6 汤钊猷.肿瘤学.上海:上海医科大学出版社,1993,1081-1083.











